Den Fascinerende Kjemien Bak Eddik og Natron Reaksjonen
I en verden full av kjemiske interaksjoner, er reaksjonen mellom edikk (eddiksyre) og natron (natriumbikarbonat) en av de mest kjente og brukte. Dette tilsynelatende enkle samspillet skjuler en kompleks kjemi som er både lærerik og praktisk anvendelig i hverdagen. Fra spennende vitenskapelige eksperimenter til effektive rengjøringsmetoder, er forståelsen av denne reaksjonen nøkkelen til å utnytte dens fulle potensial. Denne omfattende guiden vil dykke dypt inn i de vitenskapelige prinsippene som styrer reaksjonen, utforske et bredt spekter av praktiske bruksområder, diskutere viktige sikkerhetsaspekter, og gi deg en grundig forståelse av hvorfor denne kjemiske kombinasjonen er så allsidig og kraftfull.
Grunnleggende Kjemiske Prinsipper: Syre-Base Reaksjonen

Reaksjonen mellom eddik og natron er et klassisk eksempel på en syre-base reaksjon. For å fullt ut forstå hva som skjer når disse to stoffene blandes, er det viktig å ha en grunnleggende forståelse av syrer og baser på et kjemisk nivå.
Hva er en Syre?
En syre er en kjemisk forbindelse som donerer en proton (et hydrogenion, H+) i en kjemisk reaksjon. Syren i vanlig husholdningseddik er eddiksyre (CH₃COOH). Eddiksyre er en svak syre, noe som betyr at den ikke fullstendig dissosierer (deler seg opp i ioner) når den løses i vann. Likevel har den evnen til å donere et proton og reagere med baser.
Hva er en Base?
En base er en kjemisk forbindelse som aksepterer en proton (H+) i en kjemisk reaksjon. Natron, også kjent som natriumbikarbonat (NaHCO₃), er en svak base. Bikarbonationet (HCO₃⁻) i natron kan akseptere et proton fra en syre.

Den Kjemiske Reaksjonen i Detalj
Når eddiksyre (CH₃COOH) og natriumbikarbonat (NaHCO₃) blandes i vann, skjer følgende kjemiske reaksjon:
$$\text{CH}_3\text{COOH}(aq) + \text{NaHCO}_3(s) \rightarrow \text{CH}_3\text{COONa}(aq) + \text{H}_2\text{CO}_3(aq)$$
I denne reaksjonen donerer eddiksyren et proton (H+) til bikarbonationet (HCO₃⁻) fra natriumbikarbonatet. Dette fører til dannelsen av to nye produkter: natriumacetat (CH₃COONa) og karbonsyre (H₂CO₃).

Nedbrytningen av Karbonsyre
Karbonsyre (H₂CO₃) er en ustabil forbindelse som raskt brytes ned til vann (H₂O) og karbondioksidgass (CO₂):
$$\text{H}_2\text{CO}_3(aq) \rightarrow \text{H}_2\text{O}(l) + \text{CO}_2(g)$$
Det er denne produksjonen av karbondioksidgass som er ansvarlig for den observerbare boblingen og fizzingen når eddik og natron blandes. Natriumacetat (CH₃COONa) forblir oppløst i vannet.
Ionisk Perspektiv på Reaksjonen
For en dypere forståelse kan vi se på reaksjonen på et ionisk nivå. Eddiksyre i vann dissosierer delvis til acetationer (CH₃COO⁻) og hydrogenioner (H+):
$$\text{CH}_3\text{COOH}(aq) \rightleftharpoons \text{CH}_3\text{COO}^-(aq) + \text{H}^+(aq)$$
Natriumbikarbonat i vann dissosierer til natriumioner (Na+) og bikarbonationer (HCO₃⁻):
$$\text{NaHCO}_3(s) \rightarrow \text{Na}^+(aq) + \text{HCO}_3^-(aq)$$
Når disse løsningene blandes, reagerer hydrogenionene (H+) med bikarbonationene (HCO₃⁻) for å danne karbonsyre:
$$\text{H}^+(aq) + \text{HCO}_3^-(aq) \rightarrow \text{H}_2\text{CO}_3(aq)$$
Og som tidligere nevnt, brytes karbonsyren raskt ned til vann og karbondioksid:
$$\text{H}_2\text{CO}_3(aq) \rightarrow \text{H}_2\text{O}(l) + \text{CO}_2(g)$$
De tilskuende ionene i denne reaksjonen er natriumionene (Na+) og acetationene (CH₃COO⁻), som forblir i løsningen som natriumacetat.
Praktiske Bruksområder for Eddik og Natron Reaksjonen
Den kjemiske reaksjonen mellom eddik og natron har et bemerkelsesverdig bredt spekter av praktiske anvendelser, både i husholdningen og i mer spesialiserte sammenhenger. Den er verdsatt for sin evne til å produsere karbondioksid, som kan brukes til heving, rengjøring og ulike eksperimenter.
Matlaging og Baking
En av de mest kjente bruksområdene er i baking. Når eddik og natron kombineres i en deig, produseres karbondioksidgass. Disse små gassboblene fanges i deigen og får den til å heve seg, noe som resulterer i en lettere og luftigere tekstur i det ferdige bakverket. Dette er spesielt nyttig i oppskrifter som ikke inneholder gjær eller bakepulver.
Effektiv og Miljøvennlig Rengjøring
Reaksjonen mellom eddik og natron er også en kraftfull og miljøvennlig rengjøringsmetode. Kombinasjonen kan brukes til å løsne smuss, fett og flekker fra ulike overflater. Boblingen som oppstår hjelper til med å løfte partikler bort fra overflaten som rengjøres. Noen vanlige bruksområder inkluderer:
- Rengjøring av avløp: Hell natron ned i avløpet etterfulgt av eddik. Reaksjonen hjelper til med å løsne opp ansamlinger av fett og hår. Skyll med varmt vann etter en stund.
- Fjerning av fastbrent mat: En blanding av eddik og natron i en kasserolle eller panne kan hjelpe til med å løsne fastbrent mat. La det virke en stund før rengjøring.
- Rengjøring av mikrobølgeovn: En skål med eddik og vann varmet i mikrobølgeovnen kan løsne smuss, som deretter enkelt kan tørkes bort. En pasta av natron og vann kan brukes til å skrubbe vanskelige flekker.
- Fjerning av dårlig lukt: Å plassere en skål med natron i kjøleskapet eller andre områder med dårlig lukt kan absorbere lukten. En blanding av eddik og vann kan også sprayes for å nøytralisere lukt (vær forsiktig med overflater som kan skades av eddik).
- Rengjøring av fuger: En pasta av natron og litt vann eller eddik kan påføres fuger for å fjerne smuss og mugg.
Spennende Vitenskapelige Eksperimenter
Reaksjonen mellom eddik og natron er en favoritt i vitenskapelige eksperimenter, spesielt for barn og i utdanningsøyemed. Det er en visuelt engasjerende måte å demonstrere kjemiske prinsipper på en sikker og tilgjengelig måte.
Vulkaneksperimentet
Det klassiske vulkaneksperimentet er et utmerket eksempel. En modell av en vulkan lages, og inni plasseres natron. Når eddik (ofte farget rød for å ligne lava) helles over natronen, oppstår en kraftig fizzing og «utbrudd» av karbondioksidgass som ligner et vulkanutbrudd.
Ballongoppblåsing
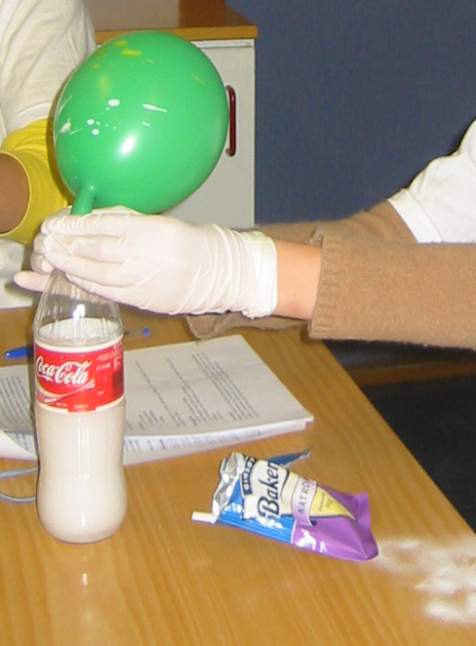
Et annet enkelt eksperiment er å fylle en ballong med natron og en flaske med eddik. Når ballongen festes over flaskeåpningen og natronen tømmes ned i eddiken, vil den produserte karbondioksidgassen blåse opp ballongen.
Andre Demonstrasjoner
Reaksjonen kan også brukes til å demonstrere prinsippet om trykk og volum for gasser, samt konseptet om kjemisk endring hvor stoffer med forskjellige egenskaper dannes.
Medisinske og Personlige Bruksområder (med forsiktighet)
Selv om det er viktig å utvise forsiktighet og konsultere helsepersonell, har eddik og natron også noen potensielle medisinske og personlige bruksområder:
- Lindring av halsbrann: Natron kan nøytralisere overflødig magesyre og gi midlertidig lindring av halsbrann. Det er viktig å bruke det i moderate mengder og være klar over potensielle interaksjoner med medisiner.
- Fotbad: En blanding av eddik og vann kan brukes som et beroligende fotbad. Eddikens antibakterielle egenskaper kan også være nyttige.
- Hårpleie: Noen mennesker bruker en blanding av eddik og natron som en naturlig måte å rense håret og fjerne produktrester. Dette bør gjøres med forsiktighet, da det kan påvirke hårets pH-balanse.
Industrielle Anvendelser
Selv om det er mindre vanlig i stor skala, kan prinsippene bak eddik og natron reaksjonen finne anvendelse i visse industrielle prosesser hvor kontrollert produksjon av karbondioksid er ønskelig.
Sikkerhetsaspekter ved Bruk av Eddik og Natron
Selv om eddik og natron generelt anses som trygge husholdningskjemikalier, er det viktig å være klar over visse sikkerhetsaspekter ved håndtering og bruk, spesielt når de blandes.
Generelle Forholdsregler
- Unngå kontakt med øyne: Både eddik og natron kan irritere øynene. Hvis kontakt oppstår, skyll grundig med vann.
- Unngå inntak i store mengder: Selv om begge stoffene finnes i matvarer, kan inntak av store mengder føre til ubehag.
- Vær forsiktig ved blanding i lukkede beholdere: Den raske produksjonen av karbondioksidgass kan bygge opp trykk og potensielt føre til at beholderen sprekker. Bland derfor alltid i åpne eller ventilerte beholdere.
Spesifikke Advarsler
- Halsbrannbehandling: Personer med visse medisinske tilstander, som høyt blodtrykk eller nyreproblemer, bør være forsiktige med å bruke natron mot halsbrann på grunn av det høye natriuminnholdet. Rådfør deg med lege.
- Reaksjonens intensitet: Mengden eddik og natron som brukes påvirker intensiteten av reaksjonen. Store mengder kan produsere en kraftig og rask gassutvikling.
- Overflatekompatibilitet: Eddik er surt og kan skade visse overflater som marmor, kalkstein og noen typer metaller. Test alltid på et lite synlig område først.

Førstehjelp
- Ved øyekontakt: Skyll øyeblikkelig med rikelig med vann i minst 15 minutter. Søk legehjelp hvis irritasjonen vedvarer.
- Ved inntak: Drikk vann for å fortynne. Søk legehjelp hvis det oppstår ubehag.
- Ved hudkontakt: Skyll huden med vann. Irritasjon er sjelden, men kan forekomme hos sensitive personer.
Faktorer som Påvirker Reaksjonen
Intensiteten og hastigheten til reaksjonen mellom eddik og natron kan påvirkes av flere faktorer:
Konsentrasjonen av Eddiksyre
Jo høyere konsentrasjon av eddiksyre i eddiken, desto mer hydrogenioner (H+) er tilgjengelig for å reagere med bikarbonationene. Dette vil føre til en raskere og kraftigere produksjon av karbondioksidgass.
Mengden Natron
Mengden natron som tilsettes vil også påvirke mengden karbondioksid som produseres. En større mengde natron vil reagere med mer eddiksyre, forutsatt at det er tilstrekkelig syre til stede.
Temperatur
Temperatur kan også spille en rolle. Generelt vil kjemiske reaksjoner skje raskere ved høyere temperaturer fordi molekylene har mer energi og kolliderer oftere og med mer kraft. Imidlertid er effekten av temperatur på denne spesifikke reaksjonen kanskje ikke like dramatisk som for andre reaksjoner som krever mer aktiveringsenergi.
Overflateareal av Natron
Hvis natron er i pulverform med et stort overflateareal, vil reaksjonen skje raskere enn hvis det er i klumper eller større krystaller, da mer av natronet vil være i kontakt med eddiken samtidig.
Omrøring
Omrøring av blandingen kan bidra til å bringe reaktantene i bedre kontakt med hverandre, noe som kan øke reaksjonshastigheten.
Variasjoner og Relaterte Reaksjoner
Selv om reaksjonen mellom vanlig husholdningseddik og natron er den mest kjente, finnes det variasjoner og relaterte reaksjoner som er verdt å nevne.

Andre Syrer og Bikarbonater
Prinsippet om en syre som reagerer med et bikarbonat for å produsere karbondioksidgass gjelder også for andre syrer og bikarbonater. For eksempel vil reaksjonen mellom sitronsyre (finnes i sitronsaft) og natron gi en lignende, men kanskje litt mindre voldsom reaksjon på grunn av